
Simpele technische experimenten zijn erg handig om met kinderen te doen, dit is samen tijd doorbrengen, vaardigheden bijbrengen en begrip door kleine ontwerpers, de basis, dat de broden, zoals in de beroemde tekenfilm, niet op bomen groeien.
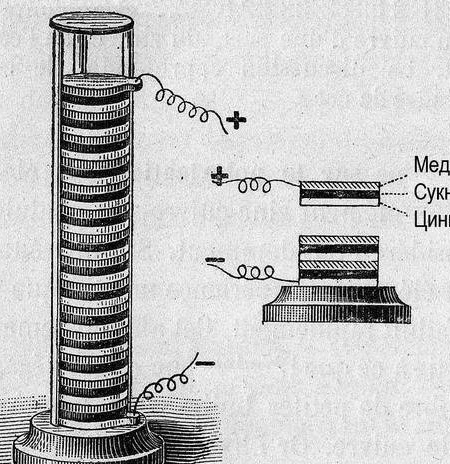
Deze keer hebben we besloten om de eenvoudigste chemische stroombron te maken en deze voor praktisch alles te gebruiken. Over de praktische toepassing gesproken, het is de moeite waard eraan te denken dat radioamateurs slechts een paar generaties geleden werden aangeboden om hun radio-ontvangers en versterkers voor batterijen te leveren, om verschillende soorten galvanische cellen of batterijen te produceren voor onafhankelijke productie. Dit zijn de elementen van Leklanshe en Popov [1] p. 9 ... 18, of een lood-potas- of gasbatterij [1], p. 22 ... 28. Verschillende elementen met een relatief hoge stroomsterkte werden aangesloten op een gloeilamp (gloeidraad van radiobuizen), tientallen kleinere elementen, op een anodebatterij waarvan de spanning 60-80 volt kon bereiken. De batterijen waren "nat" - met vloeibare elektrolyt en vereiste verzorging en onderhoud.
Dus galvanische cel, een paar woorden "hoe?" en "waarom?" Elektrische stroom treedt op wanneer metalen interageren. In dit geval treedt er een ander potentiaalverschil (spanning) op. Alessandro Volta, die in 1793 een galvanische cel (voltapool) bouwde, stelde in 1793 de relatieve activiteit van de toen bekende metalen vast: Zn, Pb, Sn, Fe, Cu, Ag, Au. De "sterkte" van de galvanische cel bleek groter te zijn, naarmate de metalen in deze rij verder uit elkaar stonden (de reeks spanningen).

Later, om de gegevens te ordenen, werd het potentieel van de "waterstofelektrode" als nulreferentie genomen. Na het potentieel van de met hem gepaarde metalen te hebben gemeten, werden de experimentele metalen achter elkaar gerangschikt. De resulterende tafel heette de "Electrochemical Series of Metal Stresses" en moet in de chemiekast naast het periodiek systeem en het portret van Dmitry Ivanovich hangen.

Een aantal metaalspanningen is een nuttig ding, in ons geval zullen we, net als Alessandro Volta, weten: hoe verder de metalen van elkaar worden gescheiden, hoe groter de spanning zal worden.
In onze experimenten gebruikten we, net als de klassiekers, koper en zink.Wanneer de platen worden ondergedompeld in de elektrolyt, tussen hen en de zinkplaat, treedt er een chemische reactie op, waardoor negatieve ladingen ophopen op de plaat en deze negatief wordt geladen. Als gevolg van de reactie in de galvanische cel lost de zinkelektrode geleidelijk op.
Op een koperelektrode worden tijdens de werking van een galvanische cel kleine waterstofbellen gevormd die het koperoppervlak isoleren van de elektrolyt. Het fenomeen wordt genoemd, in een galvanische cel is het schadelijk, ze worstelen ermee. Om de vrijgekomen waterstof te verwijderen, worden stoffen genaamd waterstof in de elektrolyt gebracht. In hun rol zijn vaak verbindingen van mangaan, kopersulfaat. In eenvoudige experimenten kan apotheekkaliumpermanganaat worden gebruikt.
Wat we voor het experiment hebben gebruikt.
Apparaten en materialen.
Voor de montage van galvanische cellen, als koperelektroden, kunt u draad, draad, folie gebruiken. Zink kan worden gewonnen uit droge elementen, gegalvaniseerde producten kunnen worden gebruikt. In plaats van zink kunt u proberen een elektrode van aluminium of ijzer te gebruiken. Natriumchloride voor elektrolyt, een beetje zachte montagedraad. Je hebt zeker een voltmeter of multimeter nodig, draadscharen, schaar. Als vaten kunnen niet-metalen containers van een geschikte maat worden gebruikt. Glas, handiger dan lichte plastic bekers - ze zijn zwaarder, stabieler en moeilijker om te stoten. Het is erg goed als er een laagstroom laagspanningsbelasting is - een eenvoudige radio, een quartzhorloge, enz.
"Hoogspanning" batterij van draad en schroeven.
Gefascineerd door de eenvoud van de details en de relatief hoge ontvangen spanning, probeerden we zo'n batterij te monteren. Hier wordt een "klassiek" paar metalen - koper-zink - gebruikt. Het idee is om gegalvaniseerde bevestigingsmiddelen te gebruiken als zinkelektrode. Gracieus. Het is duidelijk dat een dergelijk element niet is ontworpen voor langdurig gebruik - een dunne laag zink zal snel oplossen, maar dit is niet belangrijk voor een experiment op korte termijn. Maar gegalvaniseerde schroeven of tandwielen zitten overal vol.
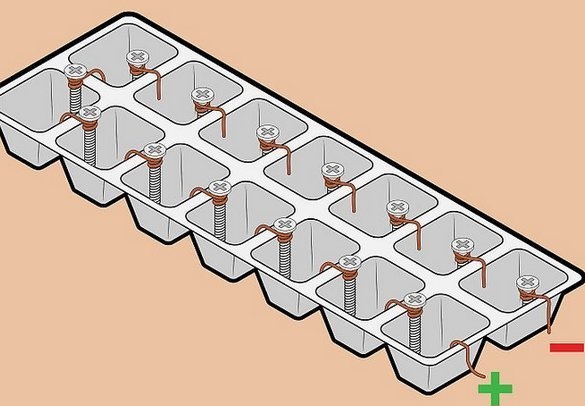
Een draad wordt ook gebruikt als koperelektrode - ook een algemeen verkrijgbaar materiaal, bovendien - de handigste installatie van elementen in een batterij - alle elementen zijn in serie verbonden - plus één met de min van de volgende. In dit geval wordt de spanning opgeteld, de stroom blijft hetzelfde.
Laten we beginnen.
Na het selecteren van het benodigde aantal verzinkte bevestigingen van de gewenste lengte, vonden we een geschikte koperdraad. Dit is een wikkeldraad in vernisisolatie. De diameter van de draad is ongeveer 0,5 mm.

Pole reinigt de vernisisolatie meerdere keren met moeite door de draad door een dubbelgevouwen schuurhuid van gemiddelde grootte te trekken.


Vervolgens bereidt hij een paar elektroden voor - onder de kop van een zelftappende schroef, wikkelt hij twee of drie windingen strak en snijdt het overtollige af.

Batterijassemblage - een bak werd gebruikt als bak om ijs in te vriezen. Je kunt cellen van snoepjes in dozen gebruiken, maar ze zijn subtieler. Nadat we de elektroden op de wanden tussen de cellen hebben geïnstalleerd, vullen we de containers met elektrolyt. We gebruikten een oplossing van tafelzout - een eetlepel met een glijbaan van 0,5 liter warm water. Voor het vullen is het erg handig om een medische spuit te gebruiken.


We hebben nog een paar schroeven voor de elektroden gevonden en elementen aan de batterij toegevoegd, dat is wat we hebben. De spanning bij een belasting met hoge impedantie (ingangsweerstand van een digitale voltmeter) is aanzienlijk, maar bij elke belasting, hoe merkbaar ook, daalt deze aanzienlijk.
Probeer het te doen soortgelijke galvanische cel (batterij) met grotere elektroden.
Als container hebben we een pot van een halve liter (twee) gebruikt, er passen platen van een aanzienlijk gebied in. Als elektroden namen we dunne koperfolie en zink - de restanten van een glas uit een "droog" fabriekselement, gedemonteerd tijdens de productie van grafiet voor vuurvaste coating.

We verwijderden de restanten van gedroogde kristallijne zouten met een staalborstel en sneden twee platen met ongeveer een schaar met ongeveer hetzelfde oppervlak. Knip uit koperfolie twee bijpassende strepen. Ook met een schaar. We hebben twee paar elektroden, die onze elementen zonder verder oponthoud hebben uitgerust en hun randen op de hals van het blik hebben gebogen.


In een grotere container hebben we een elektrolyt bereid - natriumchloride, opgelost in warm water, de concentratie is hetzelfde en de voorbereide elementen worden gegoten.


We hebben de twee elementen in serie verbonden met behulp van een stuk montagedraad en twee krokodillenklemmen. Dus goed, de accuspanning ligt dicht bij de standaard "vinger", probeer te gebruiken. Een element met een spanning van 1,5 V wordt gebruikt in een elektromechanisch horloge, daarnaast is het stroomverbruik van het horloge erg klein en zal onze batterij het kunnen overmeesteren.

We hebben de standaardbatterij uit het horloge verwijderd en een stukje van de montagedraad op de terminals aangesloten. Het observeren van de polariteit (koperen plaat - "+", zink - "-"), verbond ons horloge met een geïmproviseerde batterij, voila! De klok werkt, de spanning "zakt" naar 1,3 V. De klok werkte enkele uren perfect, totdat we allemaal opschepten (hoe dan ook een tovenaar!). Daarna werden we moe.

Naar de baan.
De interne constitutie van elk kind is zodanig dat de aandacht op één onderwerp kan focussen, niet meer dan 15 ... 20 minuten, en alle lessen met kinderen moeten zo worden gepland dat ze op dat moment passen, of wisselen tussen verschillende klassen, anders worden jullie beiden gekweld.
Als belasting is het beter om dat toe te passen, of het nu beweegt of lichtgevend is - de cijfers op de voltmeter maken indruk op de geest, maar niet op het hart. Naast horloges en rekenmachines zal het zeker bewondering wekken, het werk van een zelfgemaakte batterij van een kleine radio-ontvanger (als optie - een zelfgemaakte!).
Voor langdurig gebruik moet de elektrolyt van de cellen worden beschermd tegen stof en verdamping en moet er voor de depolarizer worden gezorgd - nou ja, de pot tenminste verstoppen met een stuk plastic film met een elastische band en kaliumpermanganaat aan de elektrolyt toevoegen. Bovendien is het beter om het genoemde element van Popov onmiddellijk te verzamelen.
Naast gegalvaniseerde zelftappende schroeven, is het mogelijk om gegalvaniseerd plaatstaal te gebruiken, voor grote elementen is het handiger - tijdens het experiment kunt u een aanzienlijke stroom en kracht krijgen, wat dan ook (uw vingers in de lucht bewegen).
Lijst met gebruikte literatuur.
1. P. Strelkov. Weten en kunnen. Elektrotechnicus van Pioneer. Detgiz. 1960 jaar
2. V.S. Polosin, V.G. Prokopenko. Workshop over de methodologie van het lesgeven in scheikunde. Moscow, "Enlightenment", 1989, blz. 202,203.

