We blijven u mooie en unieke chemische experimenten presenteren die niet alleen opvallen door hun schoonheid, maar vaak ook door eenvoud. Deze keer zullen we het chemische experiment bekijken, dat gemakkelijk kan worden herhaald, wat resulteert in chemische verkeerslichten.
We bieden u de mogelijkheid om vertrouwd te raken met het ervaringsproces in de video
Wat we nodig hebben:
- glucose;
- warm water;
- natriumhydroxide;
- indicator - indigokarmijn;
- de kolf.
We gaan verder met het verkrijgen van een chemisch verkeerslicht. Eerst moeten we ongeveer 2 gram wegen. glucose.
Los gesuspendeerde glucose op in een kleine hoeveelheid heet water.
Voeg vervolgens 10 ml natriumhydroxideoplossing toe aan onze glucoseoplossing.
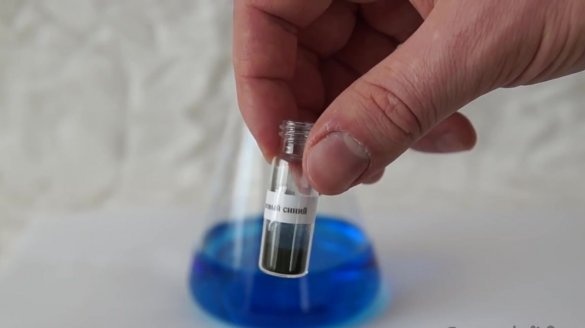
Om een kleuroplossing te maken hebben we een indicator nodig. De auteur gebruikt de indigokarmijnindicator, waarvan een kleine hoeveelheid in heet water moet worden opgelost. Giet hiervoor water in de kolf en vul daar de indicator.
Het blijkt een oplossing van verzadigd blauw te zijn.
Daarna gieten we een alkalische glucoseoplossing in de kolf en observeren we een prachtige kleurverandering: eerst wordt de oplossing groen, dan wordt hij rood en tenslotte wordt hij geel. Het zijn deze kleuren die overgangen worden en iedereen herinneren aan het bekende werk van het verkeerslicht.
Trouwens, deze reactie kan worden omgekeerd door simpelweg de oplossing te schudden. Bij lichte beweging wordt de oplossing rood en bij sterke beweging groen. Hierna gaat de reactie in de tegenovergestelde richting, dat wil zeggen dat eerst het chemische verkeerslicht groen is, dan rood en dan geel. Dit wordt verklaard door de oxidatie van de indicator met zuurstof, die in de lucht zit.
Ook kan een mooi effect worden verkregen met de "methyleenblauw" -indicator. Wanneer een alkalische glucoseoplossing wordt toegevoegd, verkleurt de indicator en wordt hij onrustig blauw.